教师公开招聘考试全国没有统一的考试形式和考试大纲,部分省份实行全省统一考试,但大部分省份还是由当地区县教育局根据当地区县各学校招聘老师人员进行汇总,然后由区县教育局和人事局统一组织招聘考试,考试形式一般分为笔试和面试,有些地区直接笔试,无需面试。上学吧教师公开招聘题库板块在教育理论综合知识、公共基础知识以及专业基础知识都精心汇编了大量的模拟试题和专项训练题,希望这些努力可以帮助到您。现在就点击安装APP刷题。以下为试卷的详细内容:
一、选择题(共25题,每题3分,共75分)参考答案见试卷末尾
1、对下列化学用语的理解正确的是( )。
A.比例模型 既可以表示甲烷分子,也可以表示四氯化碳分子
既可以表示甲烷分子,也可以表示四氯化碳分子
B.电子式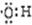 既可以表示烃基,也可以表示氢氧根离子
既可以表示烃基,也可以表示氢氧根离子
C.丙烯的最简式可表示为CH2
D.结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷
2、设NA为阿伏加德罗常数的值,下列说法不正确的是( )。
A.1molCH2=CH2分子中含有的共价键数为6NA
B.500mL0.5mol/L的NaCl溶液中微粒数大于0.5NA
C.30gHCHO与CH3COOH混合物中含C原子数为NA
D.2.3gNa与O2完全反应,反应中转移的电子数介于0.1NA和0.2NA之间
3、五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的气态化合物在水中呈碱性,C和E形成化合物CE。下列说法正确的是( )。
A.D、E、B和C四种元素简单离子半径比较:C>D>E>B
B.B、D、E简单气态氢化物稳定性比较:B>D>E
C.E最高价氧化物对应水化物的化学式为HEO4
D.C的单质在空气中燃烧产物的化学式为CO
4、已知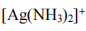 的K稳=1.12×107,则在含有0.20mol/L的
的K稳=1.12×107,则在含有0.20mol/L的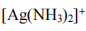 0.20mol/LNH3的混合溶液中,Ag+的浓度(mol/L)为( )。
0.20mol/LNH3的混合溶液中,Ag+的浓度(mol/L)为( )。
5、若系统经历一任意的不可逆过程,则该系统的熵变ΔS( )。
A.一定大于0
B.一定小于0
C.一定等于0
D.无法确定
6、反应①是制备SiH4的一种方法,利用其副产物可制备相应物质,有关转化关系如下: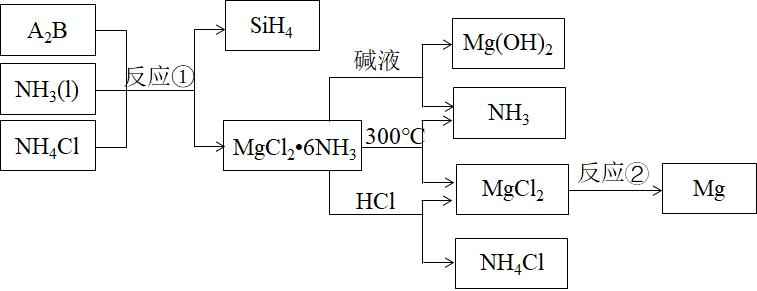 下列说法不正确的是( )。
下列说法不正确的是( )。
A.A2B的化学式为Mg2Si
B.NH3、NH4Cl可以循环使用
C.反应①中参加反应的NH3和NH4Cl的物质的量之比为1∶1
D.反应②中每生成24gMg转移2mol电子
7、溶液中除铁时还常用NaClO3作氧化剂,在较小的pH条件下最终生成一种浅黄色的黄铁矾钠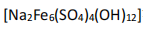 沉淀除去。下图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域。下列说法不正确的是( )。
沉淀除去。下图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域。下列说法不正确的是( )。
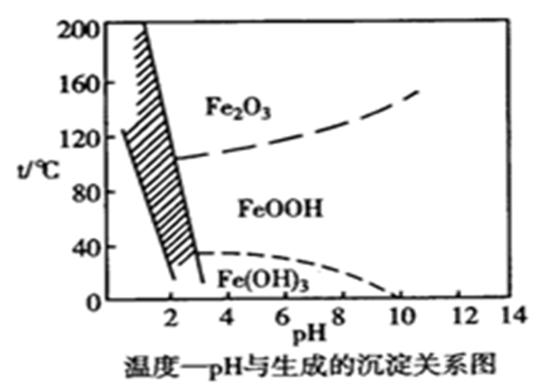
A.工业生产黄铁矾钠,温度控制在85~95℃pH=1.5左右
B.pH=6,温度从80℃升高至150℃体系得到的沉淀被氧化
C.用氯酸钠在酸性条件下氧化Fe2+离子方程式为: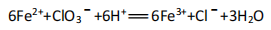
D.在25℃时溶液经氧化,调节溶液pH=4,此时溶液中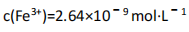
8、下列关于文献记载的说法正确的是( )。
A.《天工开物》中“世间丝麻裘褐皆具素质”,文中“丝、麻”的主要成分都是蛋白质
B.《肘后备急方》中“青蒿一握,以水二升渍,绞取汁”,该提取过程属于化学变化
C.《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”,描述的是升华和凝华过程
D.《本草纲目》中“用浓酒和糟入甑,蒸令气上,用器承滴露”,涉及的实验操作是蒸馏
9、25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-lgc(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]
A.b线表示Fe(OH)2饱和溶液中的变化关系,且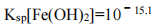
B.当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中: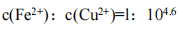
C.向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D.除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO
10、下列说法正确的是( )。
A.用盐酸标准溶液测定NaOH溶液浓度滴定实验中,滴定前无气泡而滴定后有气泡,会使测定值偏高
B.将地下钢管与直流电源的正极相连,用来保护钢管
C.已知在101KPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为: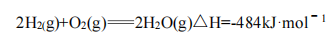
D.25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ/mol,表示稀H2SO4与KOH溶液反应的中和热的热化学方程式为: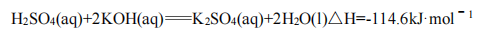
11、若要使测量误差小于+0.1%,则量取液体试样体积必须超过( )mL。
A.10
B.20
C.1
D.2
12、配制pH=10的缓冲溶液,最佳选择是( )。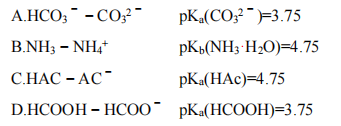
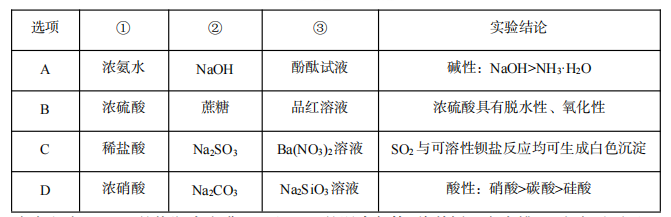
13、利用如图所示装置进行下列实验,能得出相应实验结论的是( )。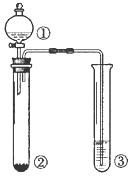
14、在容积为672mL的烧瓶中充满NO和NO2的混合气体,将其倒立在水槽里,去塞后再通入280mL氧气,恰好完全反应,且液体充满烧瓶(气体体积都已折合为标准状况下的体积),下列有关叙述正确的是( )。
A.总反应为
B.总反应为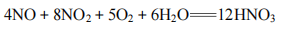
C.生成硝酸的物质的量浓度均为0.030mol/L
D.生成硝酸的物质的量浓度约为0.060mol/L
15、香兰素是重要的香料之一,它可由丁香酚经多步反应合成: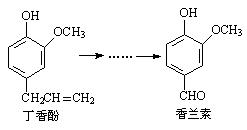 有关上述两种化合物的说法正确的是( )。
有关上述两种化合物的说法正确的是( )。
A.常温下,1mol丁香酚只能与1molBr2反应
B.丁香酚不能与FeCl3溶液发生显色反应
C.1mol香兰素最多能与3mol氢气发生加成反应
D.香兰素分子中至少有12个原子共平面
16、某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成,进行如下实验。下列有关说法正确的是( )。
A.根据上述步骤II可以得出m(Fe2O3)∶m(Cu)=1∶1
B.步骤I中减少的3g固体一定是混合物
C.步骤II中质量减少的物质一定是Cu
D.根据步骤I、II可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
17、有机物A的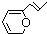 同分异构体中属于酚类的( )。
同分异构体中属于酚类的( )。
A.6种
B.7种
C.8种
D.9种
18、不能与NaHSO3饱和溶液发生加成反应生成α-羟基磺酸钠的是( )。
A.苯乙酮
B.丁酮
C.环戊酮
D.丙醛
19、现有某稀硫酸和稀硝酸的混合溶液200mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。下列分析或结果正确的是( )。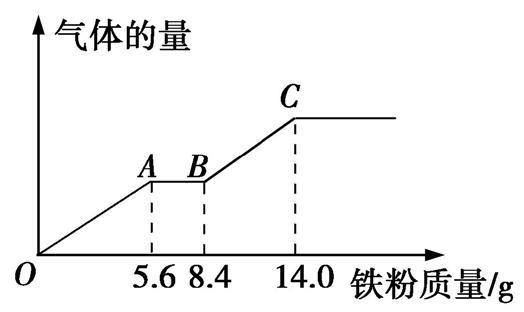
A.原混合溶液中NO3-的物质的量为0.2mol
B.OA段产生的是氢气
C.BC段产生NO
D.原混合溶液中H2SO4的浓度为1.25mol/L
20、已知某强氧化剂[RO(OH)2]2+离子被亚硫酸钠还原到较低价态。如把2.4×10-3mol[RO(OH)2]2+还原到较低价态,需12mL0.2mol/L的亚硫酸钠溶液。则反应后R的化合价为( )。
A.0
B.+2
C.+3
D.+4
21、下列对有关实验描述和解释正确的是( )。
A.SO2气体通入酸性高锰酸钾溶液中,使高锰酸钾褪色说明SO2有漂白性
B.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
C.常温下,将铝、铁片放入浓硫酸、浓硝酸中,无明显现象,说明铝、铁不与冷的浓硫酸、浓硝酸反应
D.向CuSO4溶液中加入一小块金属钠,则钠与Cu2+反应可置换出铜
22、高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。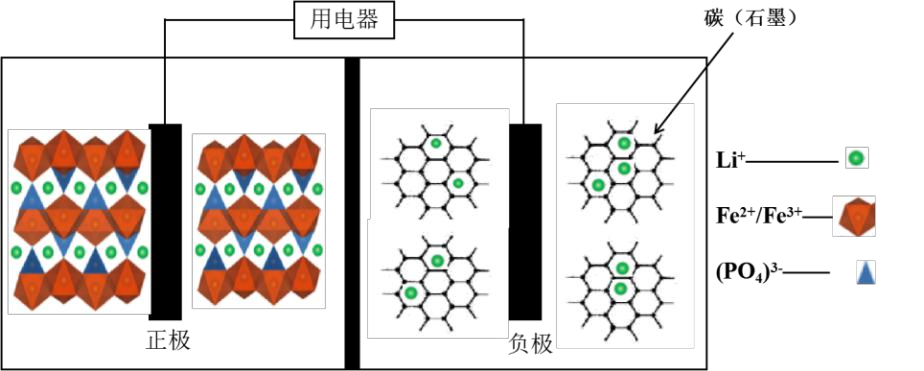 原理如下:
原理如下: 下列说法不正确的是( )。
下列说法不正确的是( )。
A.放电时,正极电极反应式: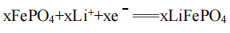
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式: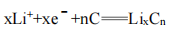
D.充电时,Li+向左移动
23、N2O5是一种新型硝化剂,在一定温度下可发生以下反应: ,T1温度时,向密闭容器中通入N2O5,部分实验数据见表下列说法中不正确的是( )。
,T1温度时,向密闭容器中通入N2O5,部分实验数据见表下列说法中不正确的是( )。
A.500s内用O2表示的平均速率为1.48×10-3mol/(L.s)
B.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1 C.T1温度下N2O5的平衡转化率为50% D.平衡后其它条件不变,将容器的体积压缩到原来的一半,则再平衡时c(N2O5)>5.00mol/L 24、Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O。当产物n(NO2)∶n(NO)=1∶1时。下列说法正确的是( )。 A.1molCu2S参加反应时有8mol电子转移 B.参加反应的n(Cu2S)∶n(HNO3)=1∶5 C.反应中Cu2S既作氧化剂,又作还原剂 D.产物n[Cu(NO3)2]∶n[CuSO4]=1∶1 25、不能正确表示下列变化的离子方程式是( )。 参考答案: 【一、选择题】 1~5 CDCBD 6~10 CBDAC 11~25点击安装“教师招聘题库APP”查看答案 如果这样刷题不过瘾,请立即安装APP刷题,历年真题、高质量模拟题应有尽有。